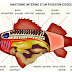
Les laryngites
Définition :
Ces affections se caractérisent par une
inflammation de la muqueuse tapissant les cartilages du larynx.
Etiologie :
La laryngite est une affection fréquente chez le
cheval de course.
Un certain nombre de conditions favorisent l’apparition d’une
laryngite ou d’une épiglottite:
- Les
affections virales comme la grippe et la rhinopneumonie dont la contagion est très importante,
- Les
traumatismes de la muqueuse par un corps étranger ou par un fourrage grossier,
- L’inhalation
de substances irritantes,
- Un
phénomène allergique,
- Le
déplacement dorsal du voile du palais.
Une laryngite peut apparaître de façon isolée, mais elle est
le plus souvent associée à une inflammation du reste de l’appareil respiratoire
supérieur.
Symptômes :
La
laryngite se caractérise par une toux fréquente, sèche, quinteuse qui se
manifeste essentiellement à l’exercice notamment au contact de l’air froid, et
pendant les repas (les quintes de
toux pendant les repas peuvent favoriser
la dysphagie).
A
l’examen clinique, la région laryngée est douloureuse à la palpation et les
nœuds lymphatiques inter-mandibulaires sont souvent réactionnels.
Un jetage
bilatéral séreux ou mucopurulent est
généralement présent.
Enfin, l’œdème de la muqueuse peut entraîner l’apparition d’un bruit
respiratoire inspiratoire et une intolérance à l’exercice parfois associés à
une dyspnée sévère.
Diagnostic :
Diagnostic clinique :
Une toux sèche à l’exercice, la
douleur à la palpation du larynx, l’augmentation de volume des nœuds
lymphatiques loco-régionaux sont
des signes cliniques évocateurs d’une inflammation de la région
pharyngo-laryngée.
De la
fièvre peut être présente en cas d’infection virale.
Diagnostic endoscopique :
L’endoscopie
va permettre l’inspection directe de la muqueuse laryngée.
En cas de laryngite ou
d’épiglottite, une hyperhémie de la muqueuse est présente,
parfois associée à la présence de follicules lymphoïdes hyperplasiés et des
sécrétions à la face dorsale de
l’épiglotte. Il arrive que la pointe de l’épiglotte soit ulcérée et laisse voir
le cartilage ainsi qu’un tissu de granulation en formation.
L’épiglottite est souvent
associée à un déplacement dorsal du voile du palais (75% des cas) et parfois à
une déviation de l’axe épiglottique (55% des cas).
Traitement :
Le traitement fait d’abord appel
à la mise en place de mesures hygiéniques et à l’association d’un traitement
médical local et général :
Une mise
au repos de 7 à 14 jours peut suffire à améliorer la situation.
Une
thérapie anti-inflammatoire et antibiotique sous forme d’un spray topique que l’on applique deux fois par jour
est souvent associée au traitement hygiènique. (Utiliser un mélange de DMSO +
furacine+glycérine+prednisone). Dans les cas sévères, l’association d’un
traitement anti-inflammatoire par voie générale peut être intéressante. L’usage est d’associer la dexaméthazone et la phénylbutazone
le premier jour, puis de poursuivre le traitement avec la phénylbutazone seule
pendant 7 à 10 jours peut être.
L’HEMIPLEGIE LARYNGEE
Définition :
L’hémiplégie
laryngée, communément appelée « cornage » correspond selon le stade de la maladie, à une parésie ou une paralysie de la musculature du larynx responsable de
l’abduction et de l’adduction des cartilages aryténoïdes.
C’est sans doute la maladie du
larynx la plus fréquemment diagnostiquée.
Une grande variété de termes peut
être employée pour décrire ce syndrome. La maladie peut prendre plusieurs formes selon sa
gravité : depuis une simple anomalie de motilité des aryténoïdes, jusqu’à
l’immobilité totale des aryténoïdes et des cordes vocales. Ainsi, une
nomenclature a été proposée pour clarifier et
simplifier la terminologie relative à cette maladie :
- La
paraplégie laryngée est une paralysie bilatérale des aryténoïdes
-
L’hémiplégie laryngée est une paralysie totale et unilatérale d’un des deux cartilages aryténoïdes
- L’hémiparésie
laryngée est une paralysie partielle ou une motilité anormale des aryténoïdes.
L’aryténoïde gauche est plus
souvent atteint, mais les cas d’hémiplégie laryngée droite ou
bilatérale sont aussi rencontrés de temps à autre.
La
maladie peut survenir quel que soit l’âge du cheval. Chez le
cheval de course, elle est souvent mise en évidence à la mise à l’entraînement,
mais elle a aussi été diagnostiquée chez
de très jeunes poulains.
Physiopathogènie :
Il s’agit d’une dégénérescence, le plus souvent spontanée,
des nerfs laryngés récurrents. Plus précisément cette dégénérescence est une
axonopathie distale du nerf laryngé récurrent caractérisée par une perte des
fibres myélinisées de gros et de moyen calibre dans la partie distale du nerf.
Le nerf laryngé récurrent gauche est
souvent atteint en regard de la crosse aortique.
Le nerf laryngé récurrent innerve tous les muscles
intrinsèques du larynx sauf le muscle crico-thyroïdien, muscle tenseur des
cordes vocales qui est innervé par le
nerf laryngé crânial.
Le muscle crico-aryténoïdien dorsal constitue l’unique
abducteur des cartilages aryténoïdes. La perte de sa fonction motrice par
dénervation et son amyotrophie sont donc les causes du déplacement axial de
l’aryténoïde observé lors d’hémiplégie laryngée.
En outre il faut aussi noter que les
muscles adducteurs du larynx, c’est à dire les muscles aryténoïdien transverse,
crico-aryténoïdien latéral et ventriculaire, sont également innervés par le nerf laryngé récurrent
et semblent affectés en priorité lorsque le nerf laryngé dégénère. L’amyotrophie des muscles adducteurs qui en résulte se
traduit par une fermeture incomplète de la glotte lors de la déglutition.
Ainsi l’amyotrophie des muscles du larynx et la mal occlusion de la glotte pendant la
déglutition sont les signes précoces de la maladie.
D’autres auteurs ont évoqué l’hypothèse que cette axonopathie
dégénérative du nerf laryngé récurrent fasse partie d’une polyneuropathie qui
atteindrait toutes les fibres longues et larges du corps. Des lésions
identiques ont été retrouvées sur les nerfs longs des membres postérieurs.
Etiologie :
L’origine de cette dégénérescence n’est pas
clairement définie.
Certaines origines traumatiques ont été reconnues
telles que des injections intraveineuses de la veine jugulaire ratées. Une injection péri vasculaire d’un
produit irritant peut induire une phlébite ou un abcès jugulaire qui
provoquent une lésion secondaire du nerf laryngé récurrent
topographiquement voisin de la veine jugulaire externe.
Un traumatisme de l’encolure ou un acte chirurgical dans cette même région
peuvent également être à l’origine d’une lésion du nerf laryngé récurrent.
L’intubation orotrachéale ou nasotrachéale lors
d’une anesthésie générale peut induire une hémiplégie laryngée post-opératoire qui est souvent
transitoire.
Par ailleurs, une mycose des
poches gutturale, un abcès de gourme ou une infection virale de l’appareil
respiratoire supérieur (grippe, rhinopneumonie) peuvent induire des lésions du nerf laryngé récurrent
consécutives à l’inflammation loco-régionale qui résulte de ces affections.
Cependant le plus souvent l’hémiplégie laryngée est d’origine
idiopathique.
Parmi les facteurs incriminés les auteurs invoquent plusieurs
hypothèses :
- L’hypothèse
d’une prédisposition génétique a
été avancée et illustrée par plusieurs études. Il semble en effet que la
descendance d’un étalon atteint d’hémiplégie laryngée soit significativement
plus atteinte que la descendance d’un étalon sain.
- Un
déficit nutritionnel en thiamine a été
proposé, mais cette hypothèse n’est pas confirmée à ce
jour.
- L’inhalation
de produits toxiques comme des organophosphorés ou du plomb
semble pouvoir induire des lésions nerveuses notamment sur le nerf laryngé
récurrent.
- La
consommation de certaines plantes toxiques proches de celles
mises en causes pour le Harper Australien favoriserait aussi le développement d’une axonopathie.
- Enfin l’étroitesse
de l’espace intermandibulaire a été incriminée comme facteur prédisposant à
l’apparition d’une hémiplégie laryngée, mais cette hypothèse a été scientifiquement
réfutée.
Concernant la latéralisation de cette maladie, la prédominance des cas
d’hémiplégie laryngée gauche s’expliquerait par
des critères anatomiques.
Le nerf laryngé récurrent gauche émerge du nerf vague dans le
thorax au niveau du cœur et progresse caudalement jusqu’à l’origine de l’aorte, à proximité des nœuds lymphatiques
trachéo-bronchiques, avant de continuer son trajet
crânialement le long de l’artère carotide commune gauche en direction du
larynx. Le nerf laryngé récurrent droit prend en revanche son départ beaucoup
plus crânialement et rejoint directement
l’artère carotide commune droite pour atteindre le larynx.
Symptômes :
L’apparition des symptômes peut être progressive ou
soudaine.
Chez le cheval sain, lors d’un exercice soutenu, le larynx se
dilate sous l’action de ses muscles intrinsèques, ce qui permet une adaptation
du diamètre de la lumière laryngée à l’augmentation des flux d’air inspiratoire
et expiratoire et prévient le collapsus des cartilages laryngés lors de
l’inspiration.
Lorsque le cheval est atteint d’hémiplégie laryngée le tonus laryngé diminue. Quand la pression inspiratoire
augmente, l’aryténoïde affectée et sa corde vocale se collabent vers la lumière
du larynx ce qui induit un syndrôme d’obstruction des voies respiratoires
supérieures. La résistance au passage de l’air augmente, le flux d’air entrant
diminue et le travail nécessaire à une respiration efficace augmente considérablement.
En conséquence, le cheval devient beaucoup plus sujet à l’hypoxémie, à
l’hypercapnie et à l’acidose métabolique, ce qui se manifeste cliniquement par une intolérance à l’exercice.
Par ailleurs, la protrusion de l’aryténoïde et de la corde vocale
dans la lumière du larynx crée des turbulences et entraîne l’apparition
d’un bruit respiratoire inspiratoire à l’exercice comparable à un sifflement et
dont l’intensité augmente lorsque le travail devient soutenu ou lorsque le
cheval travaille la nuque fléchie.
Le ventricule du larynx
se retrouve béant lorsque la corde vocale est détendue. Il fait office de caisse de résonance et
contribue à amplifier ce sifflement.
L’intensité des symptômes pour un stade de gravité de la
maladie donné est variable selon les sujets. 20% des
chevaux atteints ne manifestent aucun bruit à l’exercice.
En cas de paraplégie laryngée, le cheval présente souvent une dyspnée au repos et la
détresse respiratoire est possible à tout moment. En conséquence, l’intolérance
à l’effort est sévère.
Diagnostic :
Diagnostic clinique :
Anamnèse :
Une série de questions pourront permettre d’orienter
le diagnostic :
- Depuis quand le problème est-il apparu ?
L’apparition a-t-elle été brutale ou progressive ?
- Pendant le travail, le cheval présente-t-il soudainement des signes de fatigue ?
- Les mauvaises performances se manifeste-t-elles dès
le début de l’exercice ?
- Les signes de fatigue précoce sont-ils corrélés à un
manque de souffle ?
- Le manque de souffle est-il associé à l’émission
d’un bruit inspiratoire ?
- Le bruit est-il constant ou variable ?
- Une modification de la voix de l’animal a-t-elle été
constatée ?
- Le cheval est-il en bonne forme par ailleurs ?
- Est-il sain au niveau locomoteur (33) ?
Examen du cheval au repos :
Plusieurs
manipulations vont permettre de mettre en évidence des éléments de suspicion de
la maladie.
*La palpation du muscle crico-aryténoïdien
dorsal :
On cherche à mettre en évidence l’amyotrophie de ce
muscle. La
palpation simultanée des deux côtés du
larynx permet facilement de détecter une
amyotrophie unilatérale du muscle crico-aryténoïdien dorsal. On se
placer face au cheval, la palpation étant réalisée juste en arrière des
mandibules ventralement et rostralement.
*Le test de dépression des aryténoïdes :
Ce test consiste à exercer une pression
relativement forte sur les processus musculaires des aryténoïdes ce qui induit
un bruit respiratoire inspiratoire au repos si le cheval est atteint d’hémiplégie
ou de paraplégie laryngée.
*Le Slap test (ou
test d’abduction) :
L’opérateur palpe tour à tour chaque processus
musculaire alors qu’un aide applique une claque avec le plat de la main (ou une
cravache) sur l’épaule ou le thorax du côté opposé à la palpation. Chez le cheval sain, cette
stimulation provoque une abduction
réflexe de l’aryténoïde opposé au côté de la stimulation. En revanche chez le
cheval atteint d’hémiplégie laryngée, aucune abduction n’est notée du côté
affecté.
Ce test permet de déceler les paralysies totales de
l’aryténoïde, mais plus difficilement les parésies.
Remarque : il faut savoir que le cheval devient moins réactif
si on répète la stimulation plusieurs fois. Par ailleurs le test n’est pas
fiable chez un cheval nerveux ou peureux car la stimulation n’engendrera pas
forcément de réponse même si le cheval est sain.
*Le test de grognement
Le principe de ce test repose sur le fait qu’un
cheval atteint de dénervation des adducteurs devient incapable de fermer
totalement la glotte. Cette anomalie peut être mise en évidence en menaçant le cheval au
niveau de l’abdomen ou du thorax avec une cravache. Le cheval
sain émet un « grognement » alors que le cheval malade émet un soupir
caractéristique expliqué par le fait que l’air s’échappe par la glotte
incorrectement fermée.
Examen du cheval à l’exercice :
En observant le cheval au travail, on peut mettre
en évidence quelques éléments de suspicion tels qu’un bruit respiratoire
inspiratoire qui augmente avec l’intensité de l’exercice ou une intolérance
à l’effort qui ne se manifeste pas de façon systématique et plutôt sur des
efforts de longue durée.
Diagnostic endoscopique :
Cet examen permet de préciser le diagnostic et d’exclure les autres causes de cornage. Idéalement cet examen doit être réalisé au repos et à
l’exercice, ou faute de moyens juste après l’effort.
Endoscopie au repos :
L’examen doit être réalisé autant que possible sans sédation
et sans utiliser de tord-nez, car ces derniers faussent les mouvements
spontanés des aryténoïdes.
Le but de l’examen est d’évaluer la symétrie et la
synchronisation des mouvements d’abduction et d’adduction des deux aryténoïdes, ainsi que la capacité
d’abduction maximale de chaque aryténoïde lors de l’inspiration.
L’évaluation est chiffrée selon quatre grades :
GRADE I : on observe une abduction complète et
synchrone des cartilages aryténoïdes (fonction normale).
GRADE II : Comparativement au cartilage
aryténoïde droit, le cartilage
aryténoïde gauche (ou inversement) ne se déplace pas de façon synchrone : une
hésitation, ou une vibration sont
observées durant l’inspiration ou l’expiration. En revanche les deux cartilages
atteignent l’abduction complète après une déglutition ou une inspiration forcée
provoquée par l’occlusion des naseaux.
GRADE III : L’un des deux cartilages ne se déplace
pas de façon synchrone par rapport à l’autre et l’abduction de l’un des deux cartilages est incomplète même après une inspiration forcée.
GRADE IV : le larynx est asymétrique avec une
position médiane ou paramédiane du cartilage affecté qui n’est plus capable
d’aucun mouvement.
Si l’observation des anomalies au repos est évidente pour les
cas d’hémiplégie laryngée de grade IV, pour les grades inférieurs l’endoscopie
au repos peut laisser persister un doute quant au diagnostic. Dans ce cas, ou
si le larynx a une apparence normale
avec des symptômes évocateurs d’hémiplégie laryngée, il est conseillé de
réaliser une endoscopie à l’exercice sur tapis roulant (ou juste après
l’effort) pour confirmer ou infirmer le diagnostic et faire le lien entre les anomalies observées et
l’intolérance à l’exercice.
Endoscopie à l’exercice :
Les résultats de cet examen à l’exercice ont
montré, comparés aux évaluations au repos, l’importance des deux examens pour
bien caractériser le stade de la maladie et surtout choisir un traitement
approprié.
Lorsque l’examen est réalisé
sur un cheval normal, en début d’exercice les cartilages aryténoïdes
s’ouvrent et se ferment alternativement de façon synchrone avec la respiration.
Lorsque l’intensité du travail augmente, les aryténoïdes persistent en position d’abduction pendant les deux
phases de la respiration sous l’action du muscle crico-aryténoïdien dorsal qui
maintient l’abduction et s’oppose à l’adduction provoquée par l’augmentation
des pressions négatives à l’inspiration.
Selon la sévérité de l’axonopathie et le degré de l’atrophie musculaire subséquente,
l’aptitude à maintenir cette abduction permanente est plus ou moins altérée
durant l’exercice.
Diagnostic différentiel :
Il faudra avant tout toujours corréler les observations
cliniques aux images endoscopiques. Par exemple si un cheval présente une
gêne respiratoire importante
avec des images endoscopique compatibles avec une
hémiplégie laryngée de grade I ou II il
faut suspecter une autre cause d’intolérance à l’effort telle qu’une maladie cardiovasculaire ou une anomalie de la thermorégulation.
Il en est de même pour un cheval présentant une hémiplégie laryngée de grade
III sans aucun bruit respiratoire à
l’exercice : il faudra là aussi suspecter une maladie
sous-jacente comme une boiterie ou une maladie inflammatoire chronique des petites
voies respiratoires.
La chondrite des aryténoïdes peut être confondue à
un stade d’évolution précoce avec une hémiplégie laryngée mais la présence d’un
bruit respiratoire inspiratoire et
expiratoire ou l’épaississement et la déformation du
cartilage sont des signes propres à cette autre pathologie du larynx.
Traitement :
Choix
thérapeutique selon le
grade de la maladie et les manifestations cliniques :
La décision d’intervenir chirurgicalement sur un cas
d’hémiplégie laryngée dépend avant tout
de la clinique. Deux éléments majeurs motivent l’intervention : la présence d’un bruit respiratoire à l’exercice et
l’intolérance à l’effort. Si ni l’un ni l’autre ne sont présents et que
l’hémiplégie laryngée n’est qu’une découverte d’endoscopie il faudra rester
prudent quant à la décision thérapeutique.
Cette décision peut être schématisée selon la gravité de la
maladie :
·
Les chevaux atteints d’une
hémiplégie laryngée de grade IV sont généralement
toujours cliniquement affectés par la maladie et présentent des symptômes d’intolérance à
l’exercice et/ ou un bruit respiratoire à effort. Ces
chevaux sont de bons candidats au
traitement chirurgical.
·
Les chevaux atteints d’une hémiplégie laryngée de
grade I ou II ne sont pas de bons candidats au traitement chirurgical car
ils ne présentent généralement aucune
gêne clinique à l’exercice. Si ces chevaux présentent une intolérance à l’effort ou un
bruit inspiratoire, il est préférable d’envisager de faire un bilan d’extension
et d’approfondir l’examen de l’appareil respiratoire supérieur notamment par un
examen sur tapis roulant pour rechercher la vraie cause de ces manifestations
cliniques.
·
Enfin, pour les chevaux présentant une hémiplégie
laryngée de grade III la décision thérapeutique est plus subtile. En effet chez
ces chevaux qui présentent une abduction incomplète et des mouvements
asynchrones des aryténoïdes au repos, l’évaluation du larynx à l’exercice est
décrite selon deux types cliniques : une partie de ces chevaux présente un collapsus
dynamique à l’exercice alors que les autres présentent une fonction laryngée
normale. Ces chevaux souvent
considérés comme « suspects » dans la littérature ont laissés perplexes
de nombreux cliniciens qui ne savaient pas vraiment comment interpréter ces
mouvements asynchrones des aryténoïdes. Face à cette situation il est donc
recommandé dans la mesure du possible de réaliser un examen sur tapis roulant ou faute de mieux une endoscopie
immédiatement après l’effort. Il permettra de déterminer si les symptômes sont
réellement expliqués par l’hémiplégie laryngée de grade III ou si une autre
maladie obstructive de l’appareil respiratoire supérieur est à l’origine du
bruit respiratoire et de l’intolérance à l’exercice ( par exemple une chondrite des
aryténoïdes, un déplacement
dorsal du voile du palais, un
entrapement épiglottique, ou une obstruction nasale dynamique) (25,26,
78). Dans le cas ou l’intolérance à l’exercice est le seul symptôme
cliniquement exprimé,( absence de bruit) il faut également penser à exclure les
autres causes d’intolérance à l’effort ( boiterie, mauvaise condition physique,
maladie inflammatoire chronique des
petites voies respiratoires…).Au
terme de ce bilan, si aucune autre cause que l’hémiplégie.
Laryngoplastie :
Cette technique, décrite par Marks en 1970 , a pour objectif de reconstruire la lumière laryngée dans la
position anatomique de dilatation inspiratoire maximale, et ceci dans
l’intention d’augmenter les performances sportives. Cette méthode montre toutefois de très mauvais résultats pour la diminution du
bruit respiratoire puisque la corde vocale est laissée en place. L’intervention
consiste à restaurer artificiellement l’action du muscle crico-aryténoïdien
dorsal par la mise en place d’une prothèse synthétique placée entre le
cartilage cricoïde et le processus musculaire de l’aryténoïde, ce qui stabilise
le cartilage aryténoïde en abduction. Cette chirurgie se réalise sous
anesthésie générale, le cheval étant placé en décubitus latéral ou dorsal (tête
tournée). La voie d’abord est parallèle et ventrale à la
veine linguo-faciale.
Ventriculectomie
(aussi appelée Sacculectomie) :
Cette technique fut une des premières techniques décrites
pour améliorer les chevaux atteints d’hémiplégie laryngée. Elle a pour objectif principal de
réduire le bruit respiratoire, même si elle diminue un peu également la
résistance laryngée.
L’intervention consiste à enlever le
ventricule du côté lésé, qui restant béant joue le rôle de caisse de résonance et produit ainsi
du bruit lors de l’inspiration. Il provoque également un collapsus partiel du
larynx lors de l’inspiration. Il est possible
de procéder à une ventriculectomie bilatérale pour limiter au maximum le
collapsus. Les ventricules sont coupés après avoir été
éversés.
Pour les chevaux de course, cette technique est insuffisante
compte tenu de l’intensité de l’effort.
Au contraire elle peut être préférée et suffisante pour les
chevaux de trait, de hunter, de CSO ou de dressage ; en effet l’effort fourni
est moindre, et le bruit reste le principal inconvénient. Cette chirurgie ne
nécessite pas forcément que le cheval soit placé sous anesthésie générale. La voie d’abord de cette technique consiste en une
laryngotomie ventrale.
Cette technique est décrite également par voie endoscopique
avec utilisation du laser, elle demande alors une excellente habileté et
expérience du chirurgien.


.jpg)




.jpg)